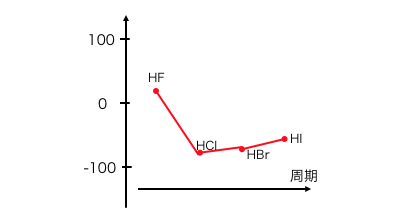
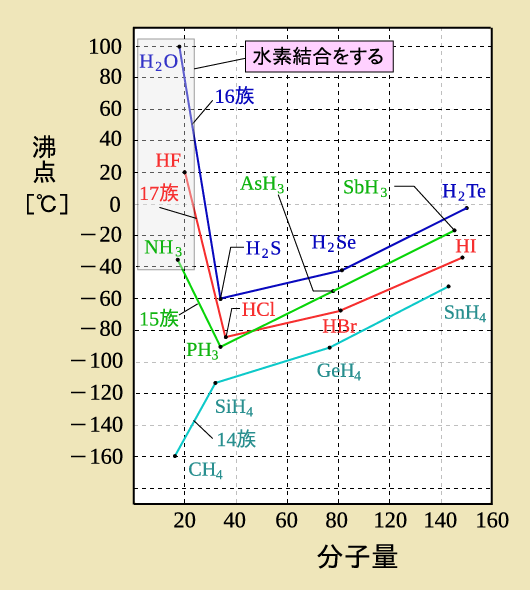
ハロゲン 化 水素 沸点 - 高等学校化学I/非金属元素の単体と化合物/ハロゲン
2 塩素 1774 年,スウェーデンの化学者シェーレ K. Br 臭素 名前の由来は、 ギリシャ語のbromos(刺激臭・悪臭)から。
純度は低いと思いますが、風呂場のような狭く閉ざされた環境で混ぜてしまうと、塩素によって中毒を起こしてしまうので、注意して下さい。
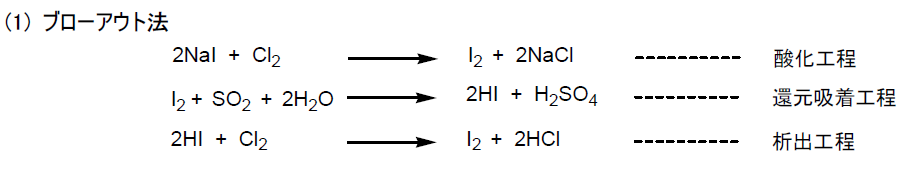
このことから、ヨウ素よりも塩素のほうが酸化力が強いことが分かる。
減圧留去し、クルードをカラム精製により87%で得た。
第四級アンモニウム塩 TBACl,TBAB を加えても良いです。
フッ素は淡黄色の気体で激しい刺激臭があり,空気よりも重い。
At アスタチン 名前の由来は、 ギリシャ語のastatos(不安定)から。
もちろんカルボン酸があれば他の塩素化剤と同様に酸塩化物が生成してしまうので注意です。
塩素は多くのビニル・プラスチック製品に含まれている。
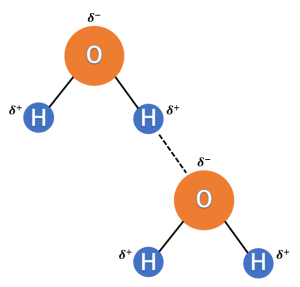
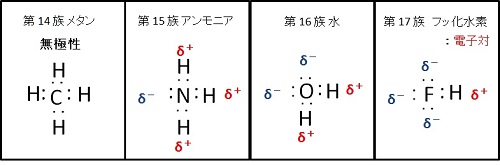
この違いから、ハロゲン化水素は共有結合、ハロゲン化アルカリ金属はイオン結合をします。
たとえば、ヨウ化カリウム水溶液に塩素を加えると、ヨウ素は酸化されて単体となる。
また、これらはいずれもチオ硫酸ナトリウム水溶液によく溶ける。
昇華性があり、加熱すると固体から液体にならず直接気体となる。
工業的には,海水のにがり中にある臭化物を塩素で酸化して製造する。
様々な分野で活躍しているが、扱いには十分注意が必要。
脱水反応のため、どを使って生成した水を除去すると効率的にハロゲン化できます。
HとF/O/Nが結合したとき、 H-F : 電気陰性度の差は1.78 H-O : 電気陰性度の差は1.24 H-N : 電気陰性度の差は0.88 となります。
名称 次亜塩素酸 亜塩素酸 塩素酸 過塩素酸 化学式 HClO HClO 2 HClO 3 HClO 4 性質 殺菌・漂白作用 殺菌・漂白作用 強力な酸化剤 塩は爆発性 さらし粉 さらし粉(化学式: CaCl ClO ・H 2O または Ca ClO 2)は、次亜塩素酸イオンを含むため、その酸化作用により漂白剤や殺菌剤として広く用いられている。
範囲外? ジオールなどポリオール類の変換にも有用です。
直塗りってこわくね・・・。
合成は簡便で、アルコールにハロゲン化チオニルを溶媒量あるいは化学量論量加えて室温~還流させて得ます。
塩化ホスホリルはピリジンと用いて光学純度を保ったまま塩化アルキルに変換可能です。
酸化力がものすごく強いので水と激しく反応します。
中性条件で進行し、穏やかに進行するため、嵩高いアルコールでも脱離反応が起こりにくいため有用です。
- 関連記事
2021 lentcardenas.com